神经退行性疾病的新靶标和新药发现
M1胆碱受体介导基底前脑斜角带核垂直区域的胆碱能神经元与海马体齿状回背侧神经元形成的单突触连接是引起阿尔茨海默病患者认知障碍最关键的神经环路,选择性增强该区域M1胆碱受体功能可以有效改善认知,但亚型间的高度保守性使得选择性增强M1胆碱受体功能极其困难,而下游信号通路的多样性又使得靶标干预变得更为复杂。解决问题的关键是深刻理解M1胆碱受体的结构与功能,以及获得具有信号通路选择性增强活性的调控剂。
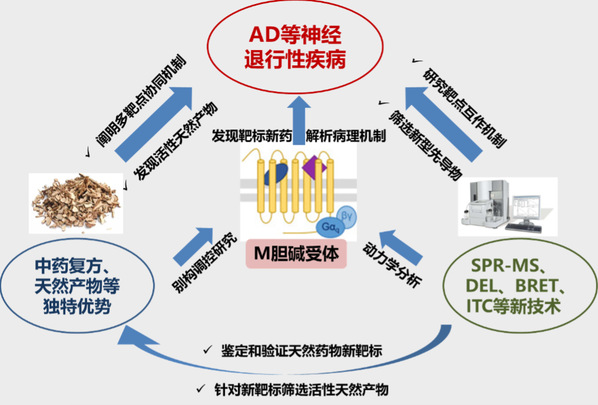
本研究方向利用天然产物具备高度结构多样性的优势解析M1胆碱受体等神经退行性疾病关键靶标的分子调控机制,探究具有特殊结构和活性的天然产物及其衍生物调控M1胆碱受体等重要靶标的结构生物学机制,发展基于分子探针的高通量筛选及药效评价模型;建立国内领先的SPR技术公共服务平台实现天然药物寻靶的关键技术突破,阐明“调心方”等疗效确切的中药复方发挥抗阿尔茨海默病作用的多靶点协同机制,产出中西医结合防治神经退行疾病和机制的原创成果,具体设置课题如下:
1. 针对M1胆碱受体等神经退行性疾病关键靶标,进一步开展分子调控机制研究:
Ø 天然拟/抗胆碱药中莨菪烷母核的构效关系及结构生物学机制研究:在中药包公藤中发现具有莨菪烷母核的天然拟胆碱药包公藤甲素,而传统上阿托品等天然莨菪烷类均呈现完全相反的抗胆碱活性。以包公藤甲素为模板,设计并合成系列衍生物,评价其对M胆碱受体的亲和力及内在活性,结合分子对接、定量构效关系、分子动力学模拟等计算机模拟方法,阐明天然拟/抗胆碱药中莨菪烷母核的构效关系。筛选获得结晶,解析受体与包甲素衍生物/阿托品复合物的三维结构,阐明莨菪烷母核在激动/拮抗M胆碱受体过程中可发挥相反活性的结构生物学机制。
Ø 发展基于分子探针的高通量筛选及药效评价模型:针对活性天然产物库,基于已有的乙酰胆碱荧光探针,进一步优化获得具有M1-M5胆碱受体各亚型结合特征的探针分子,直接用于M胆碱受体药物亲和力及内在活性的高通量筛选,且可以避免使用同位素探针或者荧光染料。开发基于BRET技术的M受体下游信号通路偏向性激活的检测方法,可用于药物激活M1受体下游-Gq通路、β-arrestin、GRK通路激活的高通量评价,为针对阿尔茨海默病的M1受体药物开发提供技术支撑。
Ø 开展针对AD动物模型受损神经环路的干预研究:利用M1胆碱受体选择性调控剂干预APP/PS1等AD动物中基底前脑-海马等重点脑区的受损神经环路,结合化学遗传学等手段评价干预后对下游信号通路的活化水平及受损神经环路功能的恢复状态,利用电生理技术评估其对突触可塑性LTP/LTD的影响,通过水迷宫、新物体识别及筑巢等行为学实验评价调控剂对AD模型动物整体学习记忆功能的影响,以明确该干预手段是否可有效改善AD症状。
2. 基于表面等离子共振分析(SPR)的靶标发现及机制研究:
Ø 基于SPR-MS方法建立天然药物寻靶的关键技术体系:在大量天然药物中,有些药物的细胞水平活性乃至动物水平活性均很确切,但作用靶点未知,寻找具有特异性的靶点是天然药物研究的重点和难点。SPR技术联合MS可以从特定细胞或组织中富集靶蛋白并可分析出靶蛋白序列和丰度信息,该方法具有实时可视且特异性高的特点,对于活性明确、靶点亲和力高的天然产物尤为适用。
Ø 结合SPR-MS寻靶和网络药理学,阐明“调心方”等抗阿尔茨海默病中药复方的多靶点协同机制:林水淼教授等研制的“调心方”、“补肾方”等方剂在抗阿尔茨海默病临床试验中可改善 AD患者的认知功能,疗效确切,然而其靶点机制并不明确。结合SPR-MS寻靶和分子库构建、相似度分析、反向对接等分子模拟方法以及靶点通路相互作用分析等网络药理学方法,明确该方中的核心药效成分及其对应的靶点,阐明上述药效成分通过多个靶点发挥协同作用的分子机制。